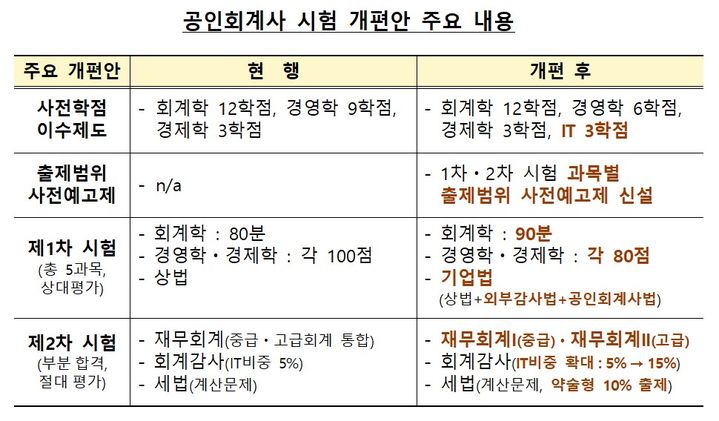
식약처, 코로나 치료제 ‘렘데시비르’ 투약범위 추가 긴급사용승인
경증·중등증의 성인과 소아(12세 이상, 40kg 이상) 환자 추가
![[AP/뉴시스] 미국이 신종 코로나바이러스 감염증(코로나19) 중증 환자를 치료하는 데 효과를 보인 항바이러스제 '렘데시비르'의 향후 3개월 생산 분량을 독점했다. 사진은 한 연구자가 렘데시비르 약물을 살펴보는 모습으로 제약사인 미국의 길리어드 사이언드가 AP통신에 제공한 것. 2020.7.2.](http://image.newsis.com/2020/04/11/NISI20200411_0016251798_web.jpg?rnd=20200702180331)
[AP/뉴시스] 미국이 신종 코로나바이러스 감염증(코로나19) 중증 환자를 치료하는 데 효과를 보인 항바이러스제 '렘데시비르'의 향후 3개월 생산 분량을 독점했다. 사진은 한 연구자가 렘데시비르 약물을 살펴보는 모습으로 제약사인 미국의 길리어드 사이언드가 AP통신에 제공한 것. 2020.7.2.
【서울=뉴시스】황재희 기자 = 식품의약품안전처는 길리어드 제약사 코로나19 치료제 ‘베클루리주’(렘데시비르)의 투약범위에 ‘중증으로 진행될 위험이 높은 경증에서 중등증의 성인과 소아(12세 이상 이고 40kg 이상) 환자’를 추가해 긴급사용 승인했다고 20일 밝혔다.
이는 질병관리청이 지난 8일 신청한데 따른 것이다.
이에 따라 기존 ‘12세 미만 또는 40kg 미만(3.5kg 이상)의 보조산소 치료가 필요한 중증 또는 폐렴이 있는 환자’에게만 허용됐던 렘데시비르 투약 범위는 ▲12세 미만 또는 40kg 미만(3.5kg 이상)의 보조산소 치료가 필요한 중증 또는 폐렴이 있는 환자 ▲중증으로 진행될 위험이 높은 경증 및 중등증의 성인 및 소아(12세 이상 이고, 40kg 이상) 환자로 확대됐다.
식약처 관계자는 “이번 긴급사용 승인은 경증에서 중등증 환자 임상시험 결과와 유럽의 허가 사례 등을 종합적으로 검토해 전문가 자문과 위원회 심의를 거쳐 결정한 것”이라고 말했다.
앞서 식약처는 지난 7일 렘데시비르의 투약 범위를 ‘성인과 12세 이상이고 40kg 이상인 소아의 보조산소 치료가 필요한 중증 또는 폐렴이 있는 입원 환자’로 변경해 허가한 바 있다.
식약처 관계자는 “앞으로도 의료제품에 대해 규제과학 전문성을 바탕으로 허가심사·긴급사용 승인할 것이며, 코로나19 극복과 국민의 일상 회복을 위해 안전하고 효과 있는 제품을 신속히 공급할 수 있도록 최선을 다하겠다”고 했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지