치매치료제 '레켐비', 치매학회서 경증환자에 사용 권고
레카네맙 적절 사용 권고안 발표
올해말 국내서 비급여 출시 예정
![[서울=뉴시스] 한국에자이 '레켐비' 로고. (사진=뉴시스 DB) photo@newsis.com *재판매 및 DB 금지](https://img1.newsis.com/2024/05/24/NISI20240524_0001558977_web.jpg?rnd=20240524180800)
[서울=뉴시스] 한국에자이 '레켐비' 로고. (사진=뉴시스 DB) [email protected] *재판매 및 DB 금지
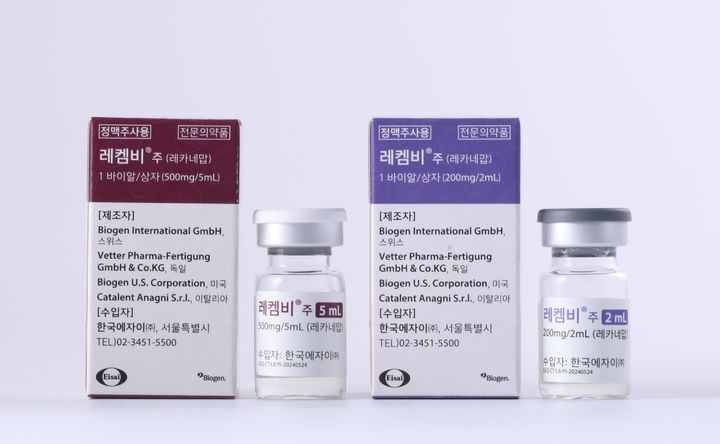
[서울=뉴시스]송연주 기자 = 올해 말 국내 출시 예정인 치매 치료 신약 '레켐비'(성분명 레카네맙)가 알츠하이머병으로 인한 경도인지장애 및 경증의 알츠하이머병 환자에게 사용이 권고됐다.
5일 제약바이오업계에 따르면 대한치매학회는 진료 현장에서 레카네맙의 치료 효과를 극대화하고 안전한 사용이 가능하도록 '레카네맙의 적절한 사용을 위한 대한치매학회 권고안'을 마련했다.
권고안에는 ▲투약 대상자 선정 ▲투약 전 필요한 검사와 준비사항 ▲투약 방법 ▲아밀로이드 관련 영상 이상(ARIA) 및 주입 관련 이상반응의 모니터링과 대처방법 등의 내용이 포함됐다.
권고안은 아밀로이드 바이오마커 양성으로 확인된 알츠하이머병으로 인한 경도인지장애와 경증의 알츠하이머병 환자에게 레카네맙 사용을 권장했다.
또 환자의 안전을 위해 필요한 전문지식을 갖춘 필수 의료인력과 인프라를 갖춘 의료기관에서 투여돼야 한다고 했다.
지난 20여 년간 약물 개발의 실패로 알츠하이머병은 대증적 치료에 기댈 수밖에 없는 불치의 영역이었으나, 레켐비의 승인으로 치료 패러다임에 변화가 일고 있다.
항아밀로이드 단클론항체인 레카네맙은 작년 7월 미국 식품의약국(FDA)에서 승인됐다. 올해 5월에는 알츠하이머병으로 인한 경도인지장애 및 경증의 알츠하이머병 성인 환자 치료에 쓸 수 있도록 국내 식품의약품안전처의 허가를 획득했다.
이 약의 3상 연구 결과, 전반적인 인지 및 기능을 측정하는 CDR-SB(Clinical Dementia Rating Sum of Boxes)를 개선시켜 알츠하이머병의 진행이 27% 지연되는 효과를 입증했다. 이 밖에 알츠하이머병 평가척도(ADAS-Cog 14), 경도인지장애 일상생활수행능력척도(ADCS MCI-ADL) 등 주요 2차 평가지표에서도 통계적으로 유의한 결과를 달성했다.
한국에자이는 레켐비를 올해 말 일단 비급여로 출시할 계획이다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지