실험쥐 없어지나…"FDA, 동물실험 안해도 신약허가 가능"
식품의약품화장품법 개정…동물실험 없이도 의약품 허가 가능
숱한 동물실험에도 신약개발 90% 실패…반대 의견 계속 제기
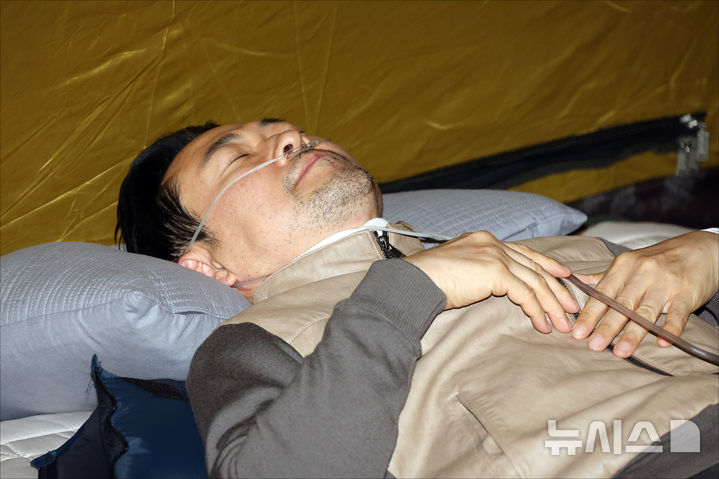
![[서울=뉴시스] *재판매 및 DB 금지](https://img1.newsis.com/2023/01/18/NISI20230118_0001178874_web.jpg?rnd=20230118163754)
[서울=뉴시스] *재판매 및 DB 금지
[서울=뉴시스]황재희 기자 = 미국 식품의약국(FDA)으로부터 의약품 허가를 받을 때 더 이상 동물실험을 하지 않아도 될 것으로 보인다.
18일 한국바이오협회 바이오경제연구센터 이슈 브리핑에 따르면, 작년 12월 미국 바이든 대통령이 서명한 2023년 통합세출법에 ‘식품의약품화장품법’ 개정이 포함되면서 앞으로는 동물실험 없이도 의약품 허가를 받을 수 있게 됐다.
FDA는 일반적으로 의약품 허가 시 생쥐와 같은 설치류 한종과 원숭이나 개와 같은 비설치류 한종에 대한 독성 시험을 요구하고 있다. 기업들은 이를 위해 매년 많은 동물실험을 진행해왔다.
그럼에도 임상시험에 들어간 신약 후보물질 10개중 9개는 실패를 하고 있어 동물실험 반대 의견이 계속해서 제기돼왔다.
이에 따라 식품의약품화장품법이 개정됐고 FDA에서 지난 80년 이상 진행해온 동물실험이 의무화에서 제외됐다.
개정된 법에는 동물실험과 같은 비임상 시험을 ‘의약품의 안전성과 효과성을 조사하는 임상시험 전 또는 그 과정 중에 시험관에서(in vitro), 컴퓨터에서(in silico), 또는 화학적으로(in chemico), 또는 비인체 생체시험(nonhuman in vivo test)에서 수행되는 시험’이라고 정의했다.
비임상 시험 예시로는 ▲세포 기반 어세이(Cell-based assays) ▲조직 칩(Organ chips) 및 미세생리시스템(Microphysiological systems) ▲컴퓨터 모델링 ▲기타 바이오프린팅(bioprinting)과 같은 비인체 또는 인체 생물학기반 시험방법과 동물실험 5가지를 예로 들었다. 동물실험 외에 4가지 방법으로 비임상 시험을 하면 되는 것이다.
또 식품의약품화장품법 개정 외에도 공중보건법을 개정해 바이오시밀러 승인 신청 시 필요한 독성 평가 규정에도 이러한 동물실험 대체법이 적용될 수 있게 했다.
다만 이 같은 변화가 의약품 허가 시스템에 있어 바로 반영될 수 있을지에 대해서는 미지수다.
아직 동물실험 대체법이 초기 단계로 향후 몇 년간 동물실험을 대체하기란 어렵다는 시각이 있기 때문이다. 특히 조직 칩 등 동물실험 대체법은 지난 10-15년간에 걸쳐 개발되고 있는 상황이다.
또 FDA가 법 개정에 따라 변화할지 여부도 아직 불확실하다. 법은 개정됐으나, 반드시 그렇게 하라는 규정은 아니기 때문이다.
FDA에 있는 독성학자들은 매우 보수적으로, 이들은 동물이 안락사된 후 모든 장기에서 잠재적인 약물의 독성 영향을 조사할 수 있다는 이유로 동물실험을 선호하고 있다.
바이오경제연구센터 관계자는 “그럼에도 불구하고 이번 법 개정은 FDA가 기업들과 동물대체 시험법이 적절한지 여부에 대해 진지하게 논의할 수 있고, 조직 칩이나 바이오프린팅과 같은 동물실험 대체법에 대한 연구개발 및 상용화가 촉진될 수 있는 법적 근거가 마련됐다는데 큰 의미를 부여할 수 있을 것”이라고 분석했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지