작년 글로벌 바이오의약품 생산량 1740만ℓ…중국·인도 무섭게 성장
작은 규모 시설 100개 이상 추가
전 세계 생산 용량 1위는 삼성바이오로직스
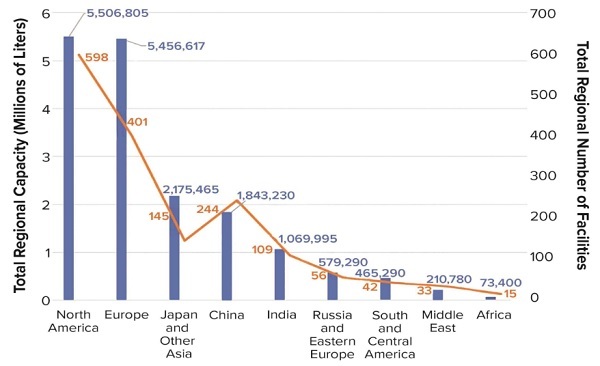
2021년 전세계 지역별 바이오의약품 생산 용량 (사진=한국바이오협회 바이오경제연구센터 제공) *재판매 및 DB 금지
【서울=뉴시스】황재희 기자 = 지난해 전 세계 바이오의약품 생산 용량은 1740만 리터로, 2018년 1650만 리터 대비 12% 증가한 것으로 나타났다.
11일 한국바이오협회 바이오경제연구센터 ‘2021년 기준 글로벌 바이오의약품 생산 용량’ 이슈 브리핑에 따르면, 지난 몇 년 간 바이오의약품 생산 인프라에 100개 이상의 시설이 추가됐으나 전체 케파(생산능력)는 크게 증가하지 않았다.
박봉현 바이오경제연구센터 책임연구원은 “바이오공정분야 전문지인 바이오프로세스 인터내셔널 자료에 따르면, 이는 상대적으로 세포 및 유전자치료제를 생산하는 작은 규모의 시설들이 늘어나고, 기존 시설 내에서 생산성 향상을 추진하고 있음을 시사한다”고 분석했다.
플랫폼별로 차지하는 비율은 포유류 기반 플랫폼이 1175만 리터로, 67.7%를 차지했다. 이어 미생물 25.8%, 혈액 및 플라즈마 4.6%, 식물 0.7% 순으로 조사됐다.
박 책임연구원은 “세포치료제, 유전자치료제 등의 첨단치료제는 바이오의약품에서 빠르게 성장하고 있으나, 전 세계 총 케파에서는 약 0.5%를 차지해 아직은 미미한 수준”이라고 말했다.
규모별로 보면, 총 1644개 시설 중 1005개(약 61%) 시설이 500리터 이상의 생산용량을 보유하고 있는 것으로 확인됐다. 이는 임상 시료를 생산할 수 있는 규모로 간주된다.
시설수 및 보유용량 면에서는 북미 및 서유럽이 압도적으로 크나, 중국과 인도가 크게 성장하고 있는 것으로 나타났다.
지역별 바이오의약품 생산 용량은 미국 및 캐나다가 598개 시설에서 550만 리터를 보유하고 있어 전체 1740만 리터의 31.7%를 차지하고 있는 것으로 조사됐다. 서유럽은 401개 시설에서 546만 리터(31.4%)를, 중국과 인도를 제외한 일본 및 기타 아시아 지역에는 145개 시설 220만 리터(12.5%)로 확인됐다.
북미에는 가장 많은 바이오의약품 제조시설이 있고, 새로운 세포·유전자치료제 CMO(위탁생산)도 많이 있으나 평균적인 생산용량은 적은 것으로 나타났다. 반면 아시아 지역의 경우 시설 수는 적으나 삼성바이오로직스와 셀트리온 등 소수의 대규모 생산시설에 집중되고 있었다.
중국은 2018년 87만 리터에서 작년 180만 리터로, 2배 이상 증가했으며, 인도는 작년 기준 110만 리터의 생산 용량을 보유하고 있는 것으로 나타났다. 시설 수로는 중국이 244개, 인도 109개다.
박 책임연구원은 “특히 중국은 제3자가 임상 및 상업용 바이오의약품을 생산할 수 있도록 규정이 변경된 이후 CMO 역량이 급격히 증가됐으며 최근 3년간 시설수가 2배가 증가했다”며 “평균 시설용량 면에 있어서는 인도에 비해 약 25%가 작지만, 인도가 주로 대규모 백신 생산인데 비해 중국은 다양한 바이오의약품 생산 플랫폼을 갖추고 적극적인 투자를 하고 있다”고 분석했다.
바이오의약품 전문 시장분석기관인 ‘BioPlan Associates’가 발표한 전 세계 시설별 바이오의약품 생산 용량 순위에서는 삼성바이오로직스(송도 1캠퍼스)가 1위를 기록한 것으로 확인됐다.
2위는 미국 소재 제넨텍·로슈, 3위는 아일랜드에 소재한 화이자, 4위는 독일에 소재한 베링거잉겔하임, 5위는 미국에 소재한 암젠, 6위는 삼성바이오로직스 4공장, 7위는 미국 암젠, 8위는 덴마크에 소재한 후지필름 다이오신스, 9위는 독일에 소재한 제넨텍·로슈, 10위는 벨기에 소재 GSK로 조사됐다.
이들 10개 시설을 위탁생산과 자체생산 시설로 구분해 보면, 위탁생산시설로는 삼성바이오로직스(한국), 베링거잉겔하임(독일), 후지필름 다이오신스(일본) 순이었고, 자체생산시설로는 제넨텍·로슈(스위스), 화이자(미국), 암젠(미국), GSK(영국) 순으로 나타났다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지