'치매신약' 레켐비, 내달 한국 상륙…안전 논란 극복할까
레켐비, 12월 국내서 출시
유럽·호주 등서 승인 불발
치매학회 "우려보다 기대"
![[서울=뉴시스] 알츠하이머 신약 레켐비 (사진=에자이 홈페이지 캡처) 2023.06.10 photo@newsis.com](https://img1.newsis.com/2023/06/10/NISI20230610_0001286537_web.jpg?rnd=20230610152612)
[서울=뉴시스] 알츠하이머 신약 레켐비 (사진=에자이 홈페이지 캡처) 2023.06.10 [email protected]
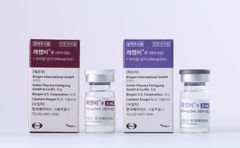
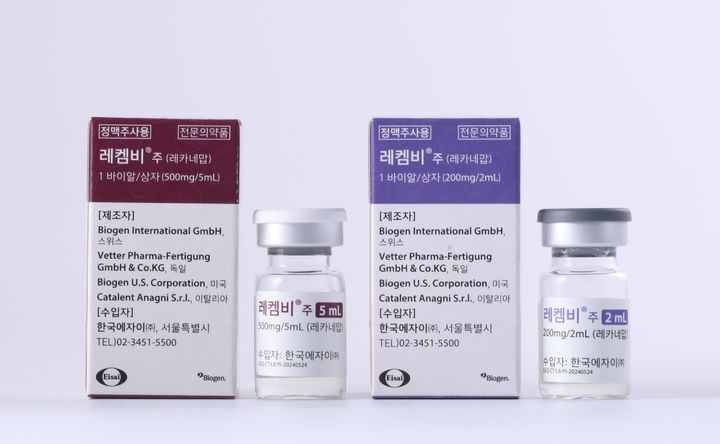
[서울=뉴시스]황재희 기자 = 글로벌제약사 에자이와 바이오젠이 개발한 알츠하이머 치료제 ‘레켐비주’(성분명 레카네맙)가 내달 국내에 출시된다. 해외에서 안전성 문제로 허가 지연 등의 문제가 불거진 가운데, 국내에서 레켐비가 얼마나 쓰일지 주목된다.
10일 관련 업계에 따르면, 레켐비는 지난 5월 국내 식품의약품안전처로부터 허가를 받아 오는 12월 출시를 앞두고 있다.
레켐비는 알츠하이머병으로 인한 경도 인지 장애나 경증 알츠하이머병 환자 치료에서 안전성과 효과성이 확인된 의약품이다. 알츠하이머병의 유력한 원인으로 알려진 뇌 아밀로이드 침착물을 감소시켜 인지기능 소실 등 질병 진행을 늦춘다.
그러나 레켐비는 안전성·효능과 관련한 논란이 이어지고 있다. 미국 식품의약국(FDA)은 레켐비를 지난해 허가했으나, 유럽과 호주 등에서는 안전성 문제를 이유로 레켐비를 허가하지 않고 있다.
유럽의약품청(EMA)은 레켐비 임상 3상에서 자기공명영상(MRI) 촬영 시 뇌에 일시적으로 부기가 확인되는 아밀로이드 관련 영상 이상(ARIA)이 나타난 부작용을 우려하며, 지난 7월 시판 허가 거부를 권고했다.
ARIA에 따라 일부 환자는 뇌출혈로 입원했으며, 임상과정에서 뇌출혈과 뇌부종으로 3명의 사망자가 발생한 점을 이유로 꼽았다. 레켐비는 투약 환자 전체 13%가 뇌부종을, 17%가 뇌출혈을 겪는 부작용이 확인된 바 있다.
호주 연방의약품 관리국(TGA)도 레켐비의 효능이 안전성보다 크지 않다는 이유로 승인을 거절했다.
이 같은 안전성 우려가 제기되자 최근에는 식약처가 레켐비를 제대로 허가했는지 여부를 두고도 논란이 됐다. 성급하게 결정한 것이 아니냐는 지적이다.
지난달 열린 국회 보건복지위원회 국정감사에서 식약처가 레켐비 허가 시 중앙약사심의위원회(이하 약심위) 검토 없이 허가를 했다는 지적이 나오자, 식약처는 모든 신약을 출시할 때 약심위가 필수는 아니며, 필요에 따라 약심위를 개최하고 있다고 설명했다.
또 레켐비는 안전성 우려와 함께 고가의 가격도 허들로 꼽힌다. 레켐비는 비급여로 출시되며, 체중에 따라 투여 용량이 달라진다. 이에 실제 환자들이 지불할 가격은 병원에 따라 다를 수 있다.
미국의 경우 70㎏ 환자의 경우 연간 3000만원의 비용이, 일본의 경우 50㎏ 환자의 연간 약값은 2000만원 수준으로 책정된 상태다.
대한치매학회, 권고안 발표…“우려보다 기대 커”
실제로 대한치매학회는 지난 4일 '레카네맙의 적절한 사용을 위한 대한치매학회 권고안'을 공개했다. 그러면서 부작용의 경우 우려할만한 수준은 아니라고 설명했다.
앞서 지난 2일 열린 대한치매학회 추계학술대회에서 최성혜 대한치매학회 이사장(인하대병원 신경과 교수)은 “레켐비가 뇌출혈이나 뇌부종 등 부작용이 있는 것은 맞지만 우려할만한 수준은 아니다”라며 “부작용 우려보다 기대감이 더 크다”고 밝혔다.
또 에자이가 올해 AAIC(알츠하이머협회 국제학술대회)에서 발표한 임상 3상인 ‘Clarity AD’ 36개월 OLE(공개연장연구) 결과에 따르면, 레켐비 치료 3년 후 주요 1차 평가 지표인 CDR-SB 점수가 ADNI(알츠하이머병 발병 예측 및 치료 효과 확인을 위해 시작된 프로젝트의 코호트 집단) 데이터를 통한 플라시보(위약) 예측군과 비교 시 -0.95까지 차이가 났다.
보통 CDR 점수가 0.5에서 1로 변화(악화)한다는 것은 환자가 자립해 최근의 사건을 기억하고, 일상생활이나 가사를 실시해 취미나 지적 관심사를 즐기는 능력이 어려워지는 단계로 해석된다.
국내 중앙치매센터 자료에 따르면, 2022년 기준 65세 이상 추정 치매 환자 수는 약 93만5000명에 달한다. 이는 65세 이상 인구 10명 중 1명가량은 치매 환자로 분류된다는 뜻이다. 또 레켐비를 쓸 수 있는 치매 전 단계로 알려진 경도인지장애 환자는 35만1117명으로, 65세 이상에서는 약 3명 중 1명이 경도인지장애인 것으로 추산된다.
한국에자이 관계자는 “에자이는 앞으로도 실제 진료 환경에서의 다양한 데이터를 통해 레켐비의 효과 및 안전성에 대한 면밀한 모니터링에 나설 전망”이라며 “레켐비 약가 역시 현재 해외 대비 적절한 수준으로 평가돼 국내에 공급될 수 있도록 본사 및 보건당국과 지속적으로 긴밀하게 협력하고 있다”고 말했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지