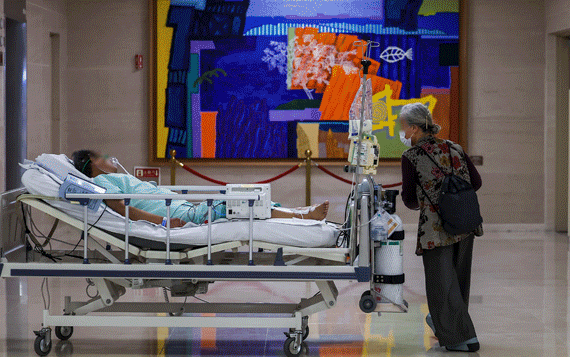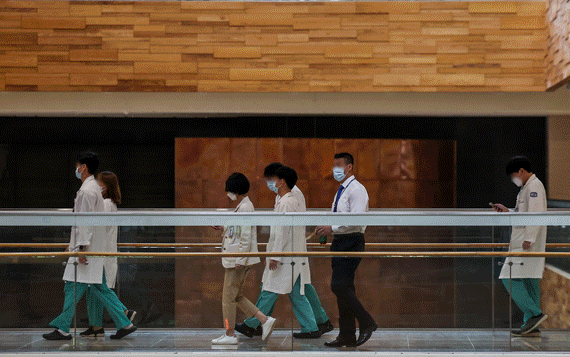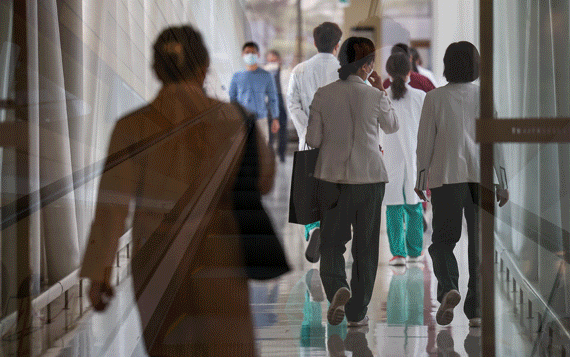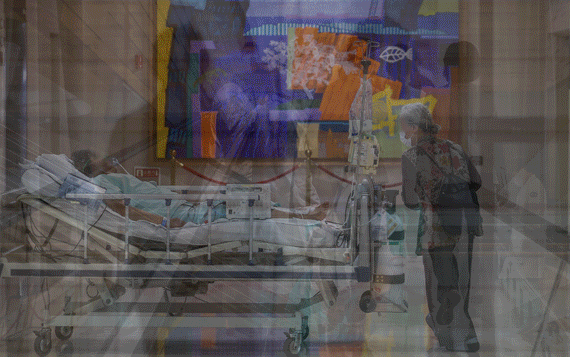식약처, WHO와 코백스 백신 심사 공조
승인 관련 의사결정에 참여
비임상·임상·품질 자료 심사
올해 코로나 백신 5건·치료제 3건 이상 도입 목표
![[세종=뉴시스]강종민 기자 = 권덕철 보건복지부 장관과 김강립 식품의약품안전처장, 정은경 질병관리청장이 25일 오후 정부세종청사에서 코로나19 조기 극복 및 포용적 일상 회복에 중점을 둔 2021년도 업무계획을 발표하고 있다. 2021.01.25. ppkjm@newsis.com](http://image.newsis.com/2021/01/25/NISI20210125_0017093790_web.jpg?rnd=20210125172649)
[세종=뉴시스]강종민 기자 = 권덕철 보건복지부 장관과 김강립 식품의약품안전처장, 정은경 질병관리청장이 25일 오후 정부세종청사에서 코로나19 조기 극복 및 포용적 일상 회복에 중점을 둔 2021년도 업무계획을 발표하고 있다. 2021.01.25.
[email protected]
식약처 김강립 처장은 25일 ‘2021년 복지부-식약처-질병관리청 업무계획 발표 브리핑’에서 “식약처는 WHO(세계보건기구)의 공동심사 요청에 따라 코백스에서 선정한 백신들에 대한 검증 작업을 진행 중이며 WHO의 승인 관련 의사결정 과정에도 참여했다”고 밝혔다.
김 처장에 따르면 식약처 직원 3명이 현재 국제 공동 심사관으로 활동 중이다.
그는 “우리 심사 전문가들이 참여했던 부분은 백신의 비임상 자료 중 주로 독성시험 관련 자료, 임상시험 자료, 품질자료 등 3개 부문에 심사 참여를 했다”며 “WHO가 긴급사용승인 관련 의견을 내는 회의에도 참여했다”고 설명했다.
이어 “이미 승인된 제품의 의사결정에 참여했을 뿐 아니라 향후 심사 과정에 계속 참여할 계획”이라고 말했다.
식약처는 올해 코로나19 백신 5건, 치료제 3건 이상의 국내 도입을 목표로 했다.
김 처장은 “백신 4건은 이미 도입 계약이 완료됐고 1건은 추가적으로 진행 중이다. 이 5개 백신의 허가를 목표로 한다”고 말했다.
이어 “또 치료제의 경우 2월 초 국내 최초 치료제에 대한 최종 결정을 예상한다. 이 제품 외에도 현재 임상시험 진행 중인 제품들을 볼 때 이 정도의 목표는 충분히 가능하리라고 본다”며 “가급적 많은 제품들이 현장에서 사용될 수 있도록 지원하겠다”고 말했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지