브릿지바이오, 1분기 연구개발비 78억…투자 확대 지속
매출액 2억원, 당기순손실 114억원

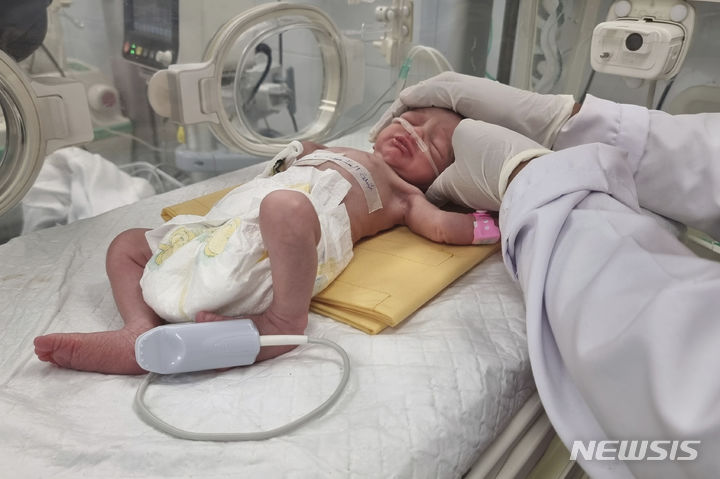
(사진=브릿지바이오테라퓨틱스 제공) *재판매 및 DB 금지
【서울=뉴시스】황재희 기자 = 혁신신약 연구개발 기업 브릿지바이오테라퓨틱스(이하 브릿지바이오)는 올해 1분기 경상연구개발비가 78억원으로, 전년 동기 대비 약 69% 증가했다고 18일 밝혔다. 매출액은 2억원, 당기순손실은 114억원이다.
브릿지바이오는 지난 17일 오후 정기 IR 기업설명회를 개최하고, 1분기 누적 결산 실적 및 신약개발 사업 진행 현황에 대해 소개했다.
현재 글로벌 미충족 의료수요가 증가하고 있는 암 질환 및 폐섬유화 질환에 집중하고 있다. 신규 상피세포 성장인자 수용체 티로신 인산화효소 억제제(EGFR)로 개발 중인 ‘BBT-176’(C797S 양성 삼중 돌연변이 대상 비소세포폐암 치료제 후보물질)은 임상 1·2상 첫 단계인 용량상승시험 추가 코호트를 통해 임상 2상 권장용량을 확정하고 효력을 추가 탐색할 예정이다.
오는 8월 세계폐암학회(IASLC 2022 WCLC)에서는 구두 발표를 통한 BBT-176의 임상 1상 주요 데이터 공개를 앞두고 있다.
작년 회사가 자체 발굴한 C797S 양성 이중 돌연변이 대상 비소세포폐암 치료제 후보물질 ‘BBT-207’은 전임상 개발을 거쳐 연내 미국과 한국에서 임상시험계획(IND)을 제출하고 내년 임상 단계에 진입하는 것을 목표로 하고 있다. 개발 중인 BBT-176과 효율적으로 연계해 사업 개발을 추진할 계획이다.
오토택신 저해제 계열 내 최초 후보물질로 개발 중인 ‘BBT-877’(특발성 폐섬유증 치료제 후보물질)은 2상 진입을 위한 미국 식품의약국(FDA)과의 막바지 협의를 앞두고 있다.
브릿지바이오 관계자는 “작년 FDA 미팅 후속 조치로 진행된 추가 동물실험을 통해 약물 독성 관련 우려를 해소한 바 있으며, 회사는 해당 결과를 바탕으로 FDA와 협의를 진행한 후 연내 약 8개 국가에서 다국가 임상 2상을 개시할 계획”이라고 말했다.
파이프라인 중 임상 단계가 가장 앞서 있는 궤양성 대장염 치료제 후보물질 ‘BBT-401’은 중·고용량 효력 확인 임상 2상을 5개국 다국가 임상으로 진행하고 있다. 전체 36명의 환자 모집을 완료하고 피험자 투약을 실시 중이다. 올해 하반기 약효에 대한 주요 결과를 발표할 계획이다.
브릿지바이오 이정규 대표이사는 이날 “암 질환 및 폐섬유화 질환 등 글로벌 미충족 의료수요가 높은 두 질환을 전략적 발판으로 삼아 당사의 핵심 역량을 더욱 강화해 나가고 있다”고 말했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지