GC녹십자 혈장치료제 의료현장 사용 확대 '쭉쭉'
아주대병원·칠곡 경북대병원 등 치료목적 사용 승인 3건 추가
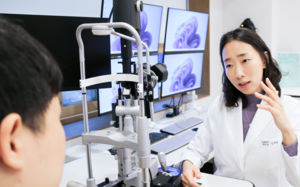
![[서울=뉴시스] GC녹십자 코로나19 혈장치료제 생산 모습(사진=GC녹십자 제공)](http://image.newsis.com/2020/10/28/NISI20201028_0000626223_web.jpg?rnd=20201028191233)
[서울=뉴시스] GC녹십자 코로나19 혈장치료제 생산 모습(사진=GC녹십자 제공)
식품의약품안전처는 지난 17일 아주대학교병원과 칠곡 경북대학교병원이 신청한 혈장 치료제 ‘GC5131A’에 대한 치료 목적 사용을 각 1건, 2건 승인했다.
이번에 총 3건이 승인되면서 ‘GC5131A’의 치료 목적 사용 승인은 총 8건으로 늘었다.
▲칠곡 경북대병원에서 3건 ▲아주대병원 2건 ▲서울아산병원 1건 ▲순천향대 부천병원 2건 등 의료기관에서 총 8건의 치료 목적 사용 승인을 받았다.
식약처는 다른 치료 수단이 없거나 생명을 위협하는 중증 환자 등 치료를 위해 임상시험용 의약품이더라도 사용할 수 있도록 하는 치료 목적 사용 승인 제도를 운영 중이다.
GC녹십자가 개발 중인 ‘GC5131A’는 현재 임상 2상 진행 중이지만 식약처 승인 하에 대체치료 수단이 없는 환자에 쓸 수 있게 됐다.
혈장 치료제의 치료 목적 승인은 대체 의약품이 없는 코로나19 환자에 치료 옵션이 확보됐다는 면에서 고무적이다.
혈장치료제는 코로나19 완치자의 혈장을 대량 수집 후 분획과정 등을 통해 혈장 속에 포함된 중화항체(면역글로불린)를 정제·농축한 제품이다. 고농도의 중화항체가 일정하게 포함돼 있다. 완치자로부터 채혈한 혈장을 대량으로 모아 혈장 내 다른 성분(알부민, 혈액응고인자 등)과 중화항체가 포함된 면역글로불린을 분리해 만들어 낸다.
현재 GC녹십자는 중앙대학교병원, 삼성서울병원 등 12개 병원에서 고위험군 환자를 대상으로 임상 2상을 진행 중이다. 전 세계적으로 코로나19 혈장치료제는 미국국립보건원(NIH) 주도의 글로벌 임상과 이스라엘 제약사 카마다(Kamada) 등 극소수가 개발 중이다.
GC녹십자 관계자는 "잇따른 치료목적 사용 승인으로 의료 현장에서 혈장 치료제의 사용 문의가 이어지고 있다"며 "앞으로 의료 현장에서 치료 목적 사용이 확대될 것으로 기대한다"고 말했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지