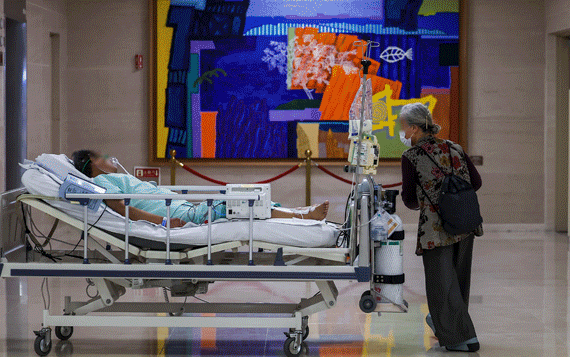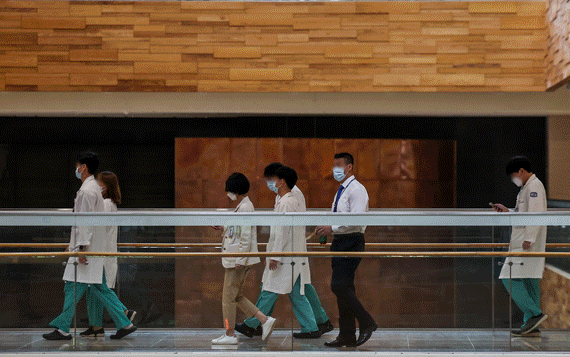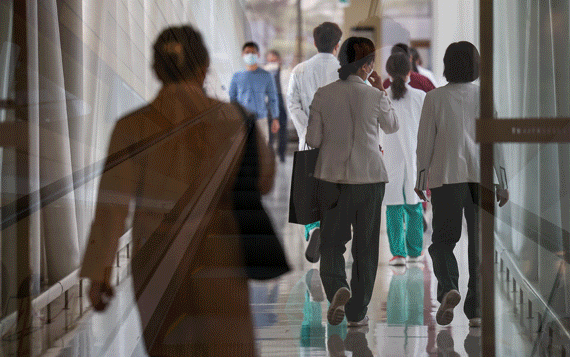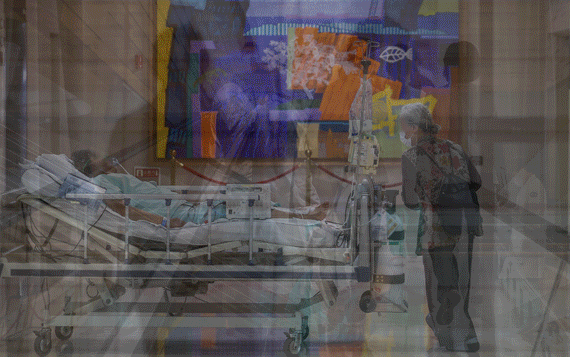혁신의료기 소프트웨어 제조기업 인증제 시행
식약처, 올해 달라지는 식품·의약품 주요 정책 소개
전시용 의료기기 용도 변경 허용

식약처는 올해부터 달라지는 식품·의약품 분야의 주요 정책을 1일 소개했다.
우선 제조·수입품목 허가를 받지 않고 전시 목적으로 승인받은 의료기기를 전시 이후, 허가를 위한 시험검사용 또는 견본용으로 용도 전환할 수 있도록 5월 중 개선할 계획이다.
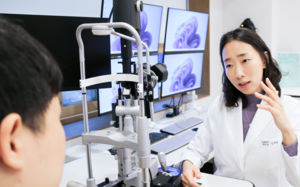
또 6월 중 우수한 혁신의료기기 소프트웨어 제조기업에 '제조기업 인증'을 부여할 계획이다. 개발 단계별로 맞춤형 기술 컨설팅을 지원한다.
인증 기업은 혁신의료기기 소프트웨어를 제조허가 받을 때 일부 제출 자료를 면제받아 신속하게 출시할 수 있게 된다.
국민보건에 중대한 영향을 미치는 의료기기에 대해선 생산·수입중단 180일 전까지 중단사유 및 중단량, 중단일정 등을 보고하도록 의무화 한다. 대체품 수급방안 마련 등 원활한 시장공급을 강구하기 위한 조치다.
식약처는 “새롭게 시행되는 제도들이 식품·의약품 안전관리를 강화하고 안전과 직결되지 않은 절차적 규제를 개선할 것”이라고 기대했다.
◎공감언론 뉴시스 [email protected]
Copyright © NEWSIS.COM, 무단 전재 및 재배포 금지